Seatimes – (ĐNA). Xạ trị là một phương pháp quan trọng điều trị ung thư phổi, có thể áp dụng cho tất cả các giai đoạn bệnh. Sự kết hợp tối ưu các tiến bộ của xạ trị với liệu pháp miễn dịch, công nghệ hình ảnh để xác định vị trí khối u theo thời gian thực, các mô hình thuật toán máy học (Machine learning) từ dữ liệu lớn, sẽ góp phần chữa trị hiệu quả, tăng thời gian sống thêm và giảm độc tính trong điều trị ung thư phổi.
Theo Tổ Chức Y Tế Thế Giới, ung thư phổi là loại ung thư gặp nhiều nhất trên Thế giới. Ở Việt Nam, trung bình cứ 100.000 dân thì có khoảng 30-40 người lớn bị mắc ung thư phổi. Trong những năm gần đây, Việt Nam đã có nhiều tiến bộ trong chẩn đoán, phát hiện sớm, cũng như các chính sách phòng chống ung thư nói chung, ung thư phổi nói riêng, đã góp phần làm giảm đáng kể tình trạng mắc mới, cải thiện hiệu quả điều trị, tăng chất lượng cuộc sống cho bệnh nhân, làm giảm gánh nặng tài chính cho người dân và chính phủ.
Ung thư phổi được chia thành 2 loại: ung thư phổi không tế bào nhỏ (NSCLC, chiếm đa số và có tiên lượng tốt hơn) và ung thư phổi tế bào nhỏ (SCLC, tỉ lệ ít hơn nhưng có tiên lượng xấu hơn). Việc điều trị ung thư phổi rất phức tạp, tùy thuộc vào tình trạng bệnh, trang thiết bị sẵn có của cơ sở điều trị, cũng như nguồn nhân lực y tế, mà có kế hoạch và phương pháp khác nhau. Phương thức điều trị thường bao gồm: phẫu thuật, xạ trị, liệu pháp toàn thân (hóa trị, liệu pháp miễn dịch, các thuốc nhắm trúng đích), và chăm sóc giảm nhẹ. Trong đó, xạ trị là một phương thức quan trọng thường được sử dụng để điều trị cho cả 2 loại ung thư phổi.
Dựa trên các báo cáo của các trung tâm ung thư trên toàn thế giới, gần 80% tất cả bệnh nhân ung thư phổi có chỉ định xạ trị, mặc dù trên thực tế, nhiều bệnh nhân không được tiếp cận phương pháp này. Hiệu quả cao của xạ trị khi được sử dụng với mục đích chữa khỏi bệnh hoặc điều trị bổ trợ sau phẫu thuật hoặc để giảm nhẹ triệu chứng trong tất cả các giai đoạn của bệnh, đã được chứng minh trong các hội nghị, bài báo trên toàn thế giới.
Những tiến bộ công nghệ gần đây đã cho phép xạ trị nhắm mục tiêu chính xác hơn vào các khối u và giảm tối đa liều liều xạ vào các mô lành xung quanh. Điều này đã mở rộng chỉ định xạ trị trong ung thư phổi và cải thiện kết quả về tăng thời gian sống thêm, tăng khả năng kiểm soát khối u tại chỗ và giảm độc tính của tia xạ.
Trong bài viết này, phóng viên Tạp chí Đông Nam Á, TS.BS Vũ Hồng Nam và Ths.BS Nguyễn Thanh Toàn đã tổng quan về các tiến bộ của công nghệ xạ trị, hiệu quả của xạ trị trong ung thư phổi và xu hướng phát triển trong tương lai của xạ trị ung thư phổi.
Những tiến bộ trong công nghệ xạ trị Chụp cắt lớp vi tính 4 chiều (4 Dimentional Computed Tomography) và xạ trị dưới hướng dẫn của hình ảnh (IGRT)
Sự phát triển nhanh chóng của các công nghệ xạ trị đã cho phép việc điều trị trở nên chính xác hơn, nhanh hơn với ít tác dụng phụ hơn. Một trong những yếu tố quan trọng tạo nên độ chính xác của việc xạ trị là công nghệ hình ảnh. Kết hợp với các dụng cụ kiểm soát nhịp thở, việc sử dụng chụp cắt lớp vi tính bốn chiều (4DCT) này cho phép đo được các chuyển động khối u, các chỉ số giao động này sau đó được đưa vào kế hoạch xạ trị để tính toán sao cho liều lượng tia xạ được phân phối chính xác đến các khối u bất kể vị trí. Việc tích hợp hệ thống hình ảnh CT với chùm tia hình nón (cone beam CT) trên các máy gia tốc (Linacs) đã làm tăng độ chính xác của tia xạ lên nhiều lần, cho phép thực hiện nhiều kỹ thuật xạ trị phức tạp.
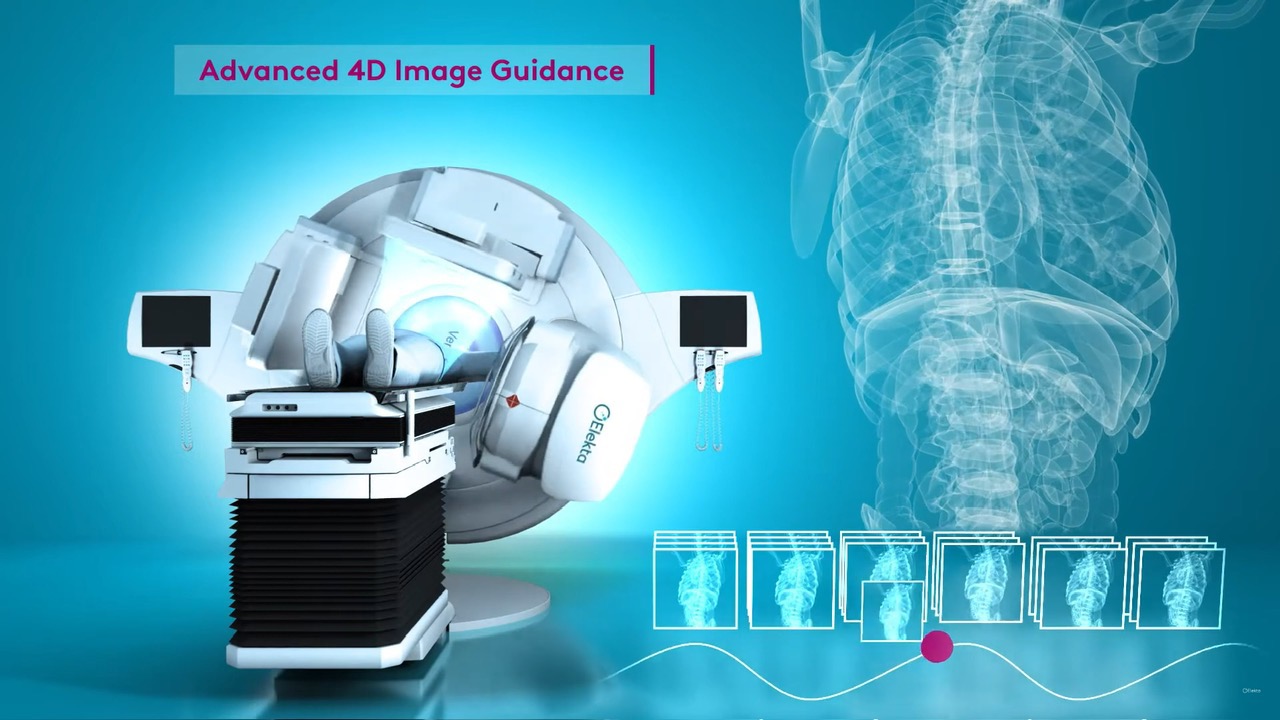
Xạ trị lập thể định vị thân (SBRT hay SABR), xạ phẫu định vị (SRS).
Sự ra đời của công nghệ hình ảnh 4DCT, kết hợp với các phương pháp cải tiến trong việc cố định thân và kiểm soát cử động hô hấp của bệnh nhân, đã cho phép xạ trị liều cao (gấp 2-3 lần thông thường), chỉ từ 1-5 lần chiếu xạ (so với khoảng 30 lần với xạ thường quy). Kỹ thuật này cho phép tăng liều xạ lên khối u, trong khi giảm thiểu tối đa lên mô phổi lành xu quanh. Từ đó làm tăng hiệu quả điều trị cho bệnh nhân. Xạ trị lập thể định vị thân hoặc xạ phẫu định vị ngày càng được áp dụng rộng rãi, không những cho nhiều loại khối u trong cơ thể, mà còn cho các loại bệnh lành tính khác (ví dụ: dị dạng mạch máu não, u dây thần kinh số 8, điều trị một số dạng loạn nhịp tim khó kiểm soát bằng thuốc thông thường).

Phương pháp xạ trị điều biến cường độ (IMRT, VMAT)
Phương pháp xạ trị điều biến cường độ (IMRT), trong đó cường độ của mỗi chùm tia được điều chỉnh, thay đổi sao cho giảm liều cho mô phổi xung quanh, trong khi vẫn đạt được liều mong muốn lên khối u. Việc thay đổi, điều biến cường độ này giúp cho giảm thiểu đáng kể tác phụ không mong muốn của xạ trị. Kỹ thuật này được thực hiện nhờ hệ thống các lá chì che chắn trường chiếu trong bộ chuẩn trực (MLC) gắn ở đầu cửa sổ phát tia của máy gia tốc, kết hợp với các thuật toán tính liều “lập kế hoạch ngược” để tối ưu liều xạ cho mỗi chùm tia hướng đến khối u. Có 2 kiểu phát chùm tia chiếu xạ: đầu phát tia cố định ở từng góc chiếu (step and shoot), và đầu phát tia vừa xoay quanh bệnh nhân và vừa phát tia xạ (VMAT). Các thế hệ máy gia tốc hiện nay đều có các tính năng này. Ngoài ra, để tăng hiệu quả của kỹ thuật này, các chuyên gia xạ trị còn kết hợp với việc theo dõi, kiểm soát sự di động của khối u theo nhịp thở, trong đó chùm tia xạ trị chỉ được bật khi khối u nằm ở một vị trí cụ thể đã xác định trước (gating). Điều này rất hữu ích cho các khối u phổi ở vùng ngoại vi có biên độ dao động lớn, dễ gây sai số lệch mục tiêu khi xạ trị.
Phương pháp xạ trị bằng chùm tia Proton, ion nặng (heavy ions)
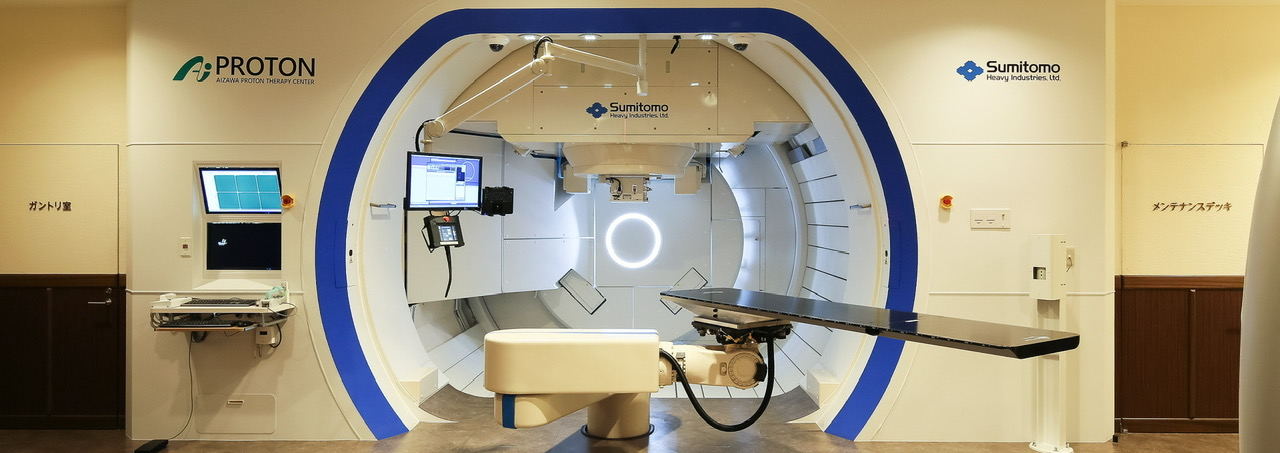
Việc ứng dụng các chùm tia proton hay các ion nặng để điều trị một số loại ung thư, trong đó có ung thư phổi, đã có từ lâu, mang lại nhiều lợi ích, giúp tăng khả năng chữa lành bệnh. Ưu điểm của các loại tia này là liều xạ hầu như chỉ tập trung vào khối u, liều xạ lên mô phổi lành xung quanh ít hơn nhiều so với chùm tia photon thông thường. Tuy nhiên, bất lợi của phương pháp này là chi phí đầu tư cho cơ sở hạ tầng rất lớn, dẫn đến giá thành cho bệnh nhân tăng cao, giảm khả năng áp dụng một cách rộng rãi liệu pháp này.
Hiệu quả, vai trò của xạ trị trong điều trị ung thư phổi.
Xạ trị cho giai đoạn sớm (giai đoạn I và II) ung thư phổi không tế bào nhỏ.
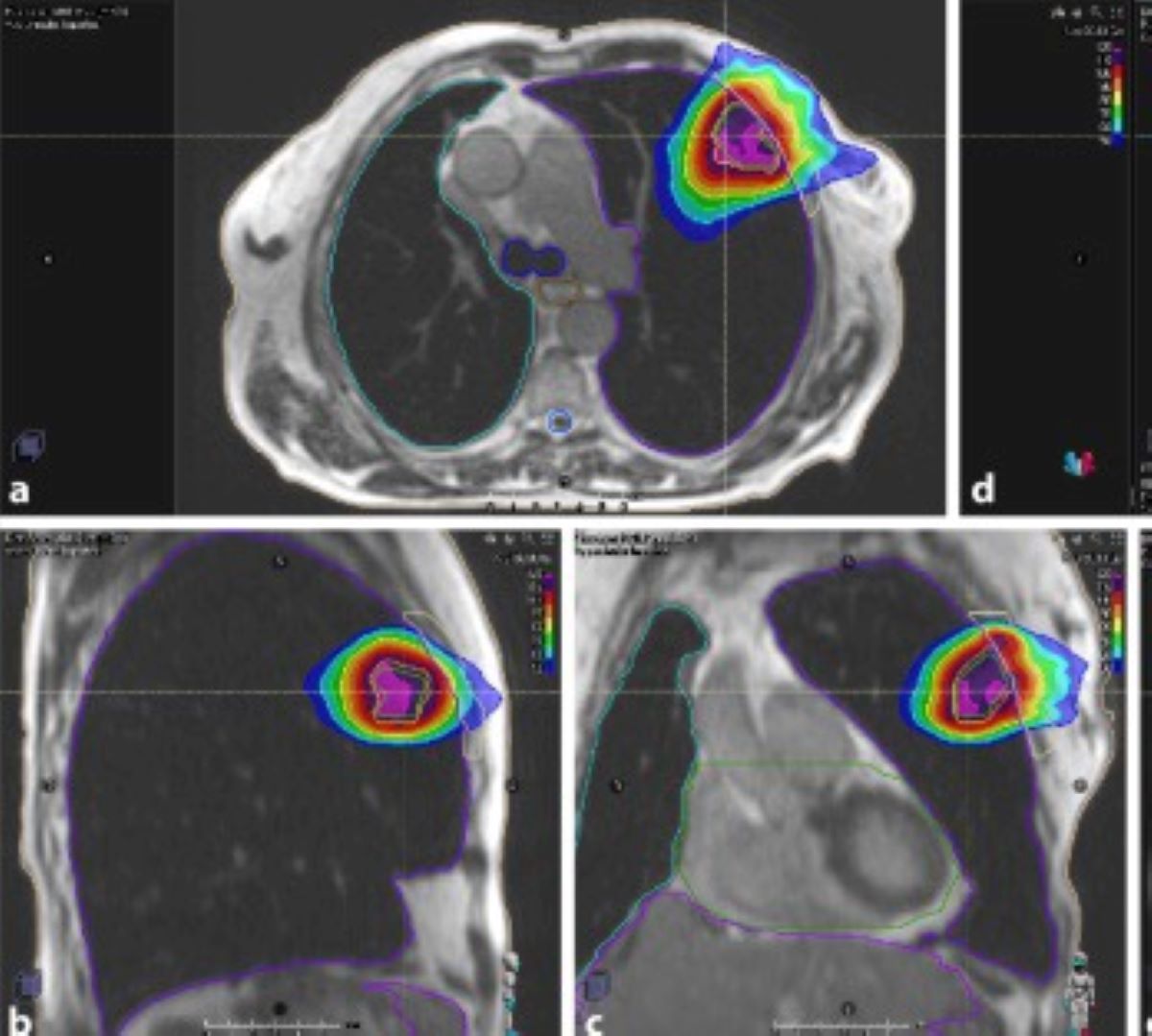
Đối với giai đoạn sớm của bệnh, phẫu thuật là lựa chọn hàng đầu, đem lại khả năng chữa khỏi cho bệnh nhân. Tuy nhiên, khoảng 15% bệnh nhân không thể phẫu thuật được, có thể do tuổi quá cao, tình trạng bệnh lý nền nặng không đảm bảo an toàn cho phẫu thuật, hay . Đối với những bệnh nhân này, xạ trị định vị thân SBRT (hay xạ phẫu SRS) là biện pháp thay thế tốt. Nhiều báo cáo kết quả điều trị ở các trung tâm xạ trị trên thế giới, cho thấy hiệu quả tương đương so với phẫu thuật, nhưng với tỉ lệ biến chứng, tác dụng phụ ít hơn so với phẫu thuật. Các báo cáo cho thấy tỉ lệ sống thêm sau 3 năm của các bệnh nhân được xạ trị (SBRT, SRS) là khoảng 80% – 85%. Ngoài ra, thời gian nằm viện ít hơn, chức năng phổi được bảo tồn hơn, ít xâm lấn hơn, không phải gây mê, bệnh nhân trở lại hoạt động hằng ngày gần như ngay sau xạ trị, đã mang lại nhiều ưu điểm của liệu pháp này.
Hình 3: Kỹ thuật xạ phẫu SBRT/ SRS với máy gia tốc có tích hợp hệ thống hình ảnh Cộng hưởng từ (MRI Linac) cho phép quan sát rõ khối u và định vị chính xác theo thời gian thực, giúp xạ trị đạt hiệu quả cao nhất, đồng thời giảm thiểu tối đa trên mô phổi lành xung quanh.
Xạ trị cho giai đoạn III ung thư phổi không tế bào nhỏ (NSCLC)
Đối với giai đoạn này, xạ trị với hóa trị liệu đồng thời sau đó điều trị bổ trợ với liệu pháp miễn dịch hay hóa trị toàn thân là phương pháp điều trị chính của đa số bệnh nhân. Tuy nhiên, do đặc điểm của giai đoạn của bệnh không còn sớm, hiệu quả của xạ trị còn hạn chế, tỉ lệ tác dụng phụ còn cao. Trong thử nghiệm Pacific, bệnh nhân NSCLC giai đoạn III, được hóa trị liệu đồng thời (54-66 Gy) sau đó được điều trị bổ trợ với durvalumab. Thời gian sống thêm trung bình là 28.7 tháng, đi kèm với tỉ lệ độc tính cao là khoảng 33%.
Đã có không ít (khoảng 10%) bệnh nhân giai đoạn này có đáp ứng tốt với phác đồ điều trị, bệnh được kiểm soát hiệu quả, một số trường hợp được phẫu thuật lấy hết khối u sau xạ trị. Từ đây cho thấy việc lựa chọn bệnh nhân sao cho phù hợp, tiên lượng đáp ứng tốt với các phương pháp điều trị kết hợp, là chìa khóa để có hiệu quả cao nhất.
Xạ trị cho giai đoạn IV ung thư phổi không tế bào nhỏ (NSCLC)
Giai đoạn IV NSCLC thường được coi là không thể chữa được. Tuy nhiên, vẫn còn một nhóm bệnh nhân có một số ít ổ di căn (oligometastases) mà việc điều trị triệt để tất cả các vị trí di căn đó, có thể dẫn đến sự sống sót lâu dài. Về cơ bản, vai trò của xạ trị trong giai đoạn này chỉ có tính chất giảm nhẹ, hỗ trợ cho liệu pháp toàn thân. Xạ trị có hiệu quả rõ ràng trong việc giảm nhẹ các triệu chứng và cải thiện chất lượng cuộc sống. Các chỉ định cụ thể cho các trường hợp khối u di căn xương gây đau, hay chèn ép đường thở gây ho, khó thở, ho ra máu, chèn ép tủy sống gây yếu liệt, hoặc di căn não.
Gần đây, có nhiều bằng chứng cho thấy việc kết hợp xạ trị (đặc biệt là xạ định vị thân/ xạ phẫu SBRT) với hóa trị nhắm trúng đích, miễn dịch liệu pháp, tế bào gốc trị liệu (cell therapy) đã mang đến nhiều hy vọng cho bệnh nhân ở giai đoạn này. Đã có không ít bệnh nhân hưởng lợi từ phương pháp trị liệu đa mô thức này, giúp tăng thêm đáng kể thời gian sống thêm, tăng sự kiểm soát khối u, hạn chế di căn thêm. Ngày càng nhiều bệnh nhân đáp ứng hoàn toàn với điều trị, thậm chí có một số trường hợp khỏi bệnh.
Xạ trị cho ung thư phổi tế bào nhỏ (SCLC) giai đoạn còn giới hạn, chưa di căn xa
Ung thư phổi tế bào nhỏ (SCLC) ít xảy ra (10%-15% ung thư phổi nối chung), nhưng có độ ác tính cao. Nhiều phương pháp điều trị đã được nghiên cứu áp dụng, tuy nhiên hiệu quả vẫn còn hạn chế.
Gần đây, với sự ra đời của các thế hệ máy xạ trị mới với cách xạ trị 2 lần/ ngày, kết hợp với các loại thuốc hóa trị, các phương pháp miễn dịch trị liệu, được áp dụng rộng rãi cho nhiều bệnh nhân hơn, đã góp phần cải thiện đáng kể gia tăng khả năng kiểm soát khối u, tạo điều kiện cho phẫu thuật can thiệp thuận lợi.
Xạ trị cho ung thư phổi tế bào nhỏ (SCLC) giai đoạn di căn xa
Đối với giai đoạn này, các phác đồ hóa trị liệu với Platinum là phương pháp điều trị chính. Mặc dù hiệu quả điều trị nói chung còn thấp, do độ ác tính cao của bệnh lý này, vẫn có nhóm bệnh nhân có đáp ứng ban đầu tốt với hóa trị, sau đó được xạ trị cho thấy hiệu quả cải thiện rõ rệt hơn hẳn so với nhóm bệnh nhân không được xạ trị kèm theo.
Kỹ thuật xạ định vị thân/ xạ phẫu (SBRT/SRS) cho các khối u ở phổi, hay các khối u di căn ở một vài vị trí, kết hợp với các liệu pháp miễn dịch, đã mang lại nhiều hy vọng cho bệnh nhân.
Xu hướng phát triển xạ trị trong tương lai.
Xạ trị và liệu pháp miễn dịch.
Nhiều phát hiện mới gần đây về xạ sinh học được đăng trên các tập san nổi tiếng chuyên ngành xạ trị (Red journal of Radiotherapy, the Lancet of radiation oncology,…) đã cho thấy xạ trị không chỉ tác động lên khối u thông qua các gốc tự do được tạo thành khi tia phóng chiếu vào, mà còn ảnh hưởng lên vi môi trường bao quanh khối u, làm thay đổi đáp ứng miễn dịch của cơ thể theo hướng tăng khả năng chống lại với tế bào u, tại vị trí nguyên phát (ở phổi) và các vị trí di căn xa. Các tác động này bao gồm định hình lại vi môi trường khối xung quanh khối u (tumor microenvironmen), làm giải phóng các hóa chất trung gian như cytokine và chemokine, dẫn đến tăng sự thâm nhập bạch cầu vào khối u, và làm tăng tính nhạy cảm của tế bào khối u với các tế bào sinh miễn dịch. Bức xạ ion hóa có thể gây ra thay đổi các con đường dẫn truyền tín hiệu tăng trưởng của khối u, ức chế sự phát triển của khối u. Ngoài ra, xạ trị còn làm tăng tính sinh miễn dịch chống lại khối u của cơ thể. Xạ trị có thể xem như là một vaccine chuyên biệt, cá nhân hóa tại chỗ rất hiệu quả, từ đó giúp nâng cao tác dụng của liệu pháp miễn dịch.
Các kết quả gần đây trong các thử nghiệm lâm sàng đã cải thiện hiệu quả, làm tăng thời gian sống thêm ở những bệnh nhân đã xạ trị trước khi bắt đầu liệu pháp miễn dịch ức chế điểm kiểm soát (ICI).
Với giả định kỹ thuật xạ định vị thân/ xạ phẫu (liều cao hơn trên mỗi tia xạ), là một chất điều hòa miễn dịch mạnh hơn so với xạ trị thông thường, các nhà khoa học đang tiến hành các nghiên cứu về sự kết hợp giữa xạ trị SBRT với liệu pháp miễn dịch trong ung thư phổi không tế bào nhỏ giai đoạn đầu, ví dụ như: thử nghiệm PACIFIC-4, ISABR; và trong giai đoạn IV, như: LONESTAR và NIVORAD. Phương pháp điều trị kết hợp này được kỳ vọng trở thành mô thức điều trị chính đối với ung thư phổi.

Các công nghệ xạ trị
Trong một thập kỷ qua, các công nghệ xạ trị đã có những tiến bộ đáng kể, làm cho việc điều trị ung thư nói chung và ung thư phổi nói riêng, có hiệu quả cao hơn, giảm độc tính và cải thiện chất lượng cuộc sống. Các công nghệ mới đầy hứa hẹn bao gồm MRI-linac, một kiểu máy gia tốc được tích hợp hệ thống chụp cộng hưởng từ kèm theo. Hệ thống MRI-Linac có thể định vị, theo dõi sự chuyển động của các khối u trong quá trình điều trị với độ chính xác cao, cho phép điều trị thích ứng theo thời gian thực, phù hợp với sự thay đổi sinh học của khối u và các mô bình thường kế cận. Phương pháp xạ trị SBRT/ SRS bằng MRI-Linac thích ứng theo thời gian thực đã được thực hiện đối với khối u ngoại vi và vùng trung tâm rốn phổi, cho phép xạ trị với liều cao hơn vào khối u, đồng thời đảm bảo trong giới hạn liều đối với các cấu trúc xung quanh . Điều này có thể làm giảm tác dụng phụ đáng kể của SBRT/SRS đối với các khối u trung tâm được xạ trị trên máy gia tốc tuyến tính thông thường.
Dữ liệu lớn và máy học (big data and Machine learning)
Ngày nay công nghệ trí thông minh nhân tạo (AI) với các thuật toán máy học (Machine learning), học sâu (deep learning), được áp dụng ngày càng nhiều trong cuộc sống. Trong điều trị ung thư phổi, ứng dụng của AI vẫn còn ở giai đoạn ban đầu, chưa khai thác nhiều tiềm năng công nghệ này. Khi các thông tin của bệnh nhân, của rất nhiều bệnh nhân được liên kết lại với nhau, tạo thành nguồn dữ liệu vô cùng lớn, phong phú và vô tận, gọi chung là “dữ liệu lớn” (big data). Nguồn dữ liệu lớn này ngày càng được phân tích, khai thác, ứng dụng trong xạ trị ung thư phổi, có thể giúp ích cho các bác sĩ lâm sàng phân loại được các nhóm bệnh nhân có nguy cơ, dự đoán được kết quả điều trị, từ đó lên kế hoạch điều trị kịp thời, đúng đối tượng bệnh nhân, và đúng phương pháp điều trị.
Bản chất của các thuật toán AI này là học hỏi (hay lấy dữ liệu) của rất nhiều bệnh nhân trước đó, rút ra các kinh nghiệm (từ các nhóm có nguy cơ thất bại điều trị, dễ tái phát), từ đó phân loại thành từng nhóm nguy cơ cao hoặc thấp, dự đoán cho bệnh nhân mới sẽ thuộc nhóm nào mà có phương án xử trí phù hợp. Điểm mạnh của ứng dụng AI này là lấy dữ liệu từ thực tế điều trị bệnh nhân trên lâm sàng vốn rất khác biệt với những bệnh nhân nghiên cứu được lựa chọn cao cho các thử nghiệm lâm sàng, có thể áp dụng cho tất cả bệnh nhân và với chi phí tương đối thấp (khác với các mô thức điều trị hiện đại có chi phí cao), để đưa ra quyết định điều trị tốt nhất cho bệnh nhân tiếp theo.
Cho đến nay, phương pháp này vẫn chưa được thử nghiệm trên thực tế lâm sàng, nhưng với tìm năng lớn, kết hợp với các kỹ thuật xạ trị, miễn dịch liệu pháp tiên tiến, sẽ góp phần tăng cao hiệu quả điều trị, cá nhân hóa hơn nữa các quyết định điều trị sao cho đúng bệnh nhân, đúng thời điểm, đúng phương pháp và phù hợp hoàn cảnh.
Do vậy, xạ trị là một phương pháp quan trọng điều trị ung thư phổi, có thể áp dụng cho tất cả các giai đoạn bệnh. Sự kết hợp tối ưu các tiến bộ của xạ trị với liệu pháp miễn dịch, công nghệ hình ảnh để xác định vị trí khối u theo thời gian thực, các mô hình thuật toán ML từ dữ liệu lớn, sẽ góp phần chữa trị hiệu quả, tăng thời gian sống thêm và giảm độc tính trong điều trị ung thư phổi.
TS.BS Vũ Hồng Nam, Ths.BS Nguyễn Thanh Toàn
n







